श्रेय: औषधीय रसायन विज्ञान जर्नल (2025)। डीओआई: 10.1021/acs.jmedchem.5c01338
कैंसर शरीर की अपनी बुनियादी अस्तित्व प्रणालियों पर कब्ज़ा करके पनपता है, जिससे बिना किसी अतिरिक्त क्षति और दुष्प्रभाव के ट्यूमर पर हमला करना कठिन हो जाता है। अब, कॉर्नेल वेइल इंस्टीट्यूट फॉर सेल एंड मॉलिक्यूलर बायोलॉजी के शोधकर्ताओं ने पता लगाया है कि एक कम आक्रामक रणनीति क्या हो सकती है जो संभावित चिकित्सीय मार्ग के रूप में वादा दिखाती है।
नए शोध में ऐसे अणुओं का पता चला है जो स्वस्थ कोशिका पर उनके पसंदीदा लगाव बिंदुओं से घातक प्रोटीन को अवरुद्ध करते हुए महत्वपूर्ण सेलुलर प्रक्रियाओं को संरक्षित कर सकते हैं। निष्कर्ष कैंसर से लड़ने के लिए एक नए दृष्टिकोण का संकेत देते हैं, जो मेलेनोमा और हड्डी के कैंसर कोशिकाओं में एपोप्टोसिस – आत्म-विनाश की प्रक्रिया – को ट्रिगर करता है।
द स्टडी, प्रकाशित 6 अक्टूबर को औषधीय रसायन विज्ञान जर्नलरसायन विज्ञान और रासायनिक जीवविज्ञान विभाग में जीवन विज्ञान में जेरेमी बास्किन, एसोसिएट प्रोफेसर और नैन्सी और पीटर मीनिग परिवार अन्वेषक के सहयोग से स्नातक छात्र नाथन फ्रेडरिक द्वारा नेतृत्व किया गया था। कला और विज्ञान महाविद्यालय में, और वेल इंस्टीट्यूट फॉर सेल एंड मॉलिक्यूलर बायोलॉजी में।
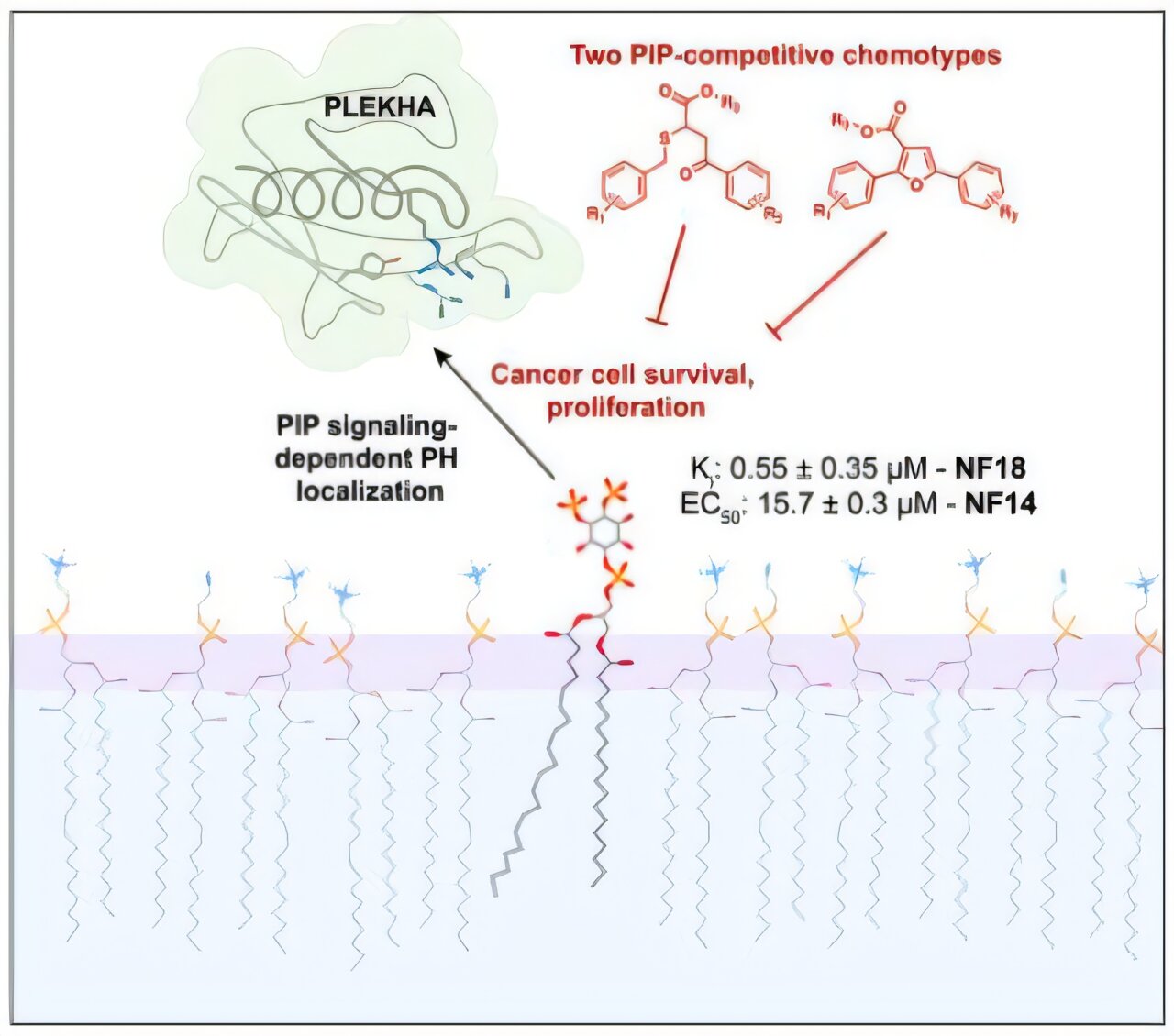
पेपर पहले यौगिकों की खोज का वर्णन करता है जो सीधे PLEKHA नामक प्रोटीन के परिवार को लक्षित करते हैं, जो कोशिका झिल्ली पर लिपिड “संदेशों” की व्याख्या करके कैंसर कोशिकाओं को बढ़ने और फैलने में मदद करते हैं।
प्रत्येक कोशिका के अंदर, फॉस्फेटिडिलिनोसिटॉल फॉस्फेट (पीआईपी) लिपिड एड्रेस लेबल की तरह काम करते हैं, प्रोटीन को सही स्थानों पर निर्देशित करते हैं और उन्हें बताते हैं कि कब कार्य करना है। कई कैंसर विभाजित होते रहने के लिए इन संकेतों का अपहरण कर लेते हैं। मौजूदा दवाएं जो पीआईपी बनाने वाले एंजाइमों को अवरुद्ध करती हैं, ट्यूमर को धीमा कर सकती हैं, लेकिन स्वस्थ कोशिकाओं को काम करने वाली महत्वपूर्ण प्रक्रियाओं को भी बाधित कर सकती हैं – विशेष रूप से चयापचय, प्रतिरक्षा और स्थिर आंतरिक वातावरण को बनाए रखने के लिए ऊतकों की क्षमता को नियंत्रित करने वाली प्रक्रियाएं। फ्रेडरिक ने कहा, ये व्यवधान गंभीर दुष्प्रभाव पैदा करते हैं।
बास्किन प्रयोगशाला की टीम ने समस्या को हल कर दिया। पीआईपी उत्पादन को बंद करने के बजाय, उनका लक्ष्य सिग्नल रिसीवर्स-प्लेकस्ट्रिन होमोलॉजी (पीएच) डोमेन को जाम करना था जो प्लेखा प्रोटीन को लिपिड अणुओं पर कब्जा करने की अनुमति देता है। फ्रेडरिक ने कहा, “हम पूरे सिस्टम को चुप कराने के बजाय लिपिड संदेश को पढ़ने से रोकना चाहते थे।”
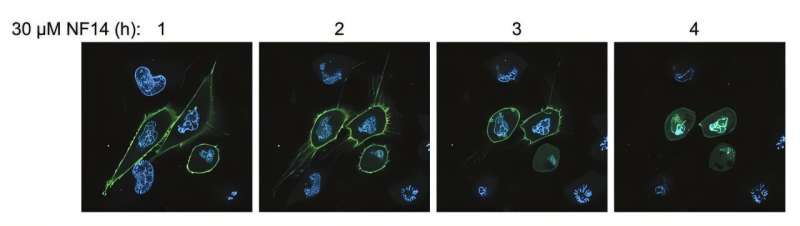
PLEKHA अणु NF14 द्वारा SK-MEL2 कोशिकाओं के प्लाज्मा झिल्ली से प्रतिस्पर्धा करते हैं। श्रेय: औषधीय रसायन विज्ञान जर्नल (2025)। डीओआई: 10.1021/acs.jmedchem.5c01338
कंप्यूटर मॉडलिंग का उपयोग करते हुए, शोधकर्ताओं ने 90,000 से अधिक दवा जैसे यौगिकों की जांच की, जो मेलेनोमा वृद्धि से जुड़े प्रोटीन PLEKHA4 के PH डोमेन में फिट हो सकते हैं। उन्होंने एनएफ1 नामक एक अणु की खोज की, जो लिपिड पॉकेट से कसकर बंधा हुआ था और अंतरिक्ष के लिए पीआईपी के साथ प्रतिस्पर्धा करता था।
इसके बाद टीम ने यह सुनिश्चित करने के लिए रासायनिक विविधताओं का निर्माण और परीक्षण किया कि यौगिक PLEKHA को अलगाव और कोशिकाओं के भीतर कितनी अच्छी तरह से बांधते हैं। एक संस्करण, एनएफ14, ने विशेष रूप से अच्छा काम किया। उन्होंने पाया कि यह एक निष्क्रिय “प्रोड्रग” के रूप में शुरू होता है जो आसानी से कोशिकाओं में प्रवेश करता है, और फिर एक बार कोशिकाओं के अंदर, यह प्राकृतिक एंजाइमों द्वारा एनएफ 1 में परिवर्तित हो जाता है, जिससे इसकी कैंसर-नाशक क्षमता सक्रिय हो जाती है।
जब मेलेनोमा और हड्डी के कैंसर कोशिका रेखाओं पर परीक्षण किया गया, तो एनएफ14 ने कोशिका झिल्ली पर प्लेखा प्रोटीन की पकड़ को बाधित कर दिया, जिससे एक श्रृंखला प्रतिक्रिया शुरू हो गई जिससे कोशिकाओं ने विभाजित होना बंद कर दिया और अपनी मृत्यु का कारण बनी। एपोप्टोटिक मार्गों के माध्यम से। महत्वपूर्ण बात यह है कि इसने कुछ प्लेखा प्रोटीन बनाने वाली कैंसर कोशिकाओं पर बहुत कम प्रभाव दिखाया, जिससे पता चलता है कि यह अपने इच्छित लक्ष्य को मार रहा है।
बास्किन ने कहा, नतीजे पहले सबूतों में से एक को चिह्नित करते हैं कि पीएच डोमेन – जिसे लंबे समय तक दवा डिजाइन के लिए बहुत मुश्किल माना जाता है – को चुनिंदा रूप से लक्षित किया जा सकता है। क्योंकि पीएच डोमेन प्रोटीन परिवारों के बीच सूक्ष्म रूप से भिन्न होता है, इस दृष्टिकोण से कम दुष्प्रभावों के साथ अधिक सटीक कैंसर दवाएं मिल सकती हैं।
बास्किन ने कहा, “इससे पता चलता है कि लिपिड सिग्नलिंग को अधिक सर्जिकल तरीके से नियंत्रित किया जा सकता है।” “पूरे रास्ते को बंद करने के बजाय, हम केवल उस हिस्से का पीछा कर सकते हैं जो कैंसर कोशिका प्रजनन में भाग ले रहा है।”
शोधकर्ता अब यह पता लगा रहे हैं कि इन यौगिकों को शक्ति और सुरक्षा के लिए कैसे अनुकूलित किया जाए। मेलेनोमा और हड्डी के कैंसर से परे, इसी तरह की रणनीतियाँ एक दिन दोषपूर्ण लिपिड सिग्नलिंग के कारण होने वाले प्रतिरक्षा या चयापचय संबंधी विकारों के इलाज में मदद कर सकती हैं।
अधिक जानकारी:
नाथन पी. फ्रेडरिक एट अल, लिपिड-प्रतिस्पर्धी प्लीक्स्ट्रिन होमोलॉजी डोमेन-युक्त परिवार ए अवरोधकों की खोज, अनुकूलन और एंटीकैंसर गतिविधि, औषधीय रसायन विज्ञान जर्नल (2025)। डीओआई: 10.1021/acs.jmedchem.5c01338
उद्धरण: शोधकर्ताओं ने कैंसर की लिपिड जीवनरेखा को काटने का नया तरीका खोजा (2025, 20 अक्टूबर) 20 अक्टूबर 2025 को लोकजनताnews/2025-10-cancer-lipid-lifeline.html से लिया गया।
यह दस्तावेज कॉपीराइट के अधीन है। निजी अध्ययन या अनुसंधान के उद्देश्य से किसी भी निष्पक्ष व्यवहार के अलावा, लिखित अनुमति के बिना कोई भी भाग पुन: प्रस्तुत नहीं किया जा सकता है। सामग्री केवल सूचना के प्रयोजनों के लिए प्रदान की गई है।